▌ 导语:
近日,5名肿瘤免疫疗法先驱荣获沃伦·阿尔珀特奖的新闻刷爆了很多人的朋友圈,大家纷纷为耶鲁陈列平教授等获奖的科学家表示祝贺。同样是在近日,另一则关于肿瘤免疫疗法的新闻也引起了许多关注:一支来自澳大利亚的科研团队通过小鼠模型,发现了用肿瘤免疫疗法治疗乳腺癌的潜在关键。这项重要研究登上了《科学》子刊《Science Translational Medicine》的封面。
▲这项研究登上了《科学》子刊《Science Translational Medicine》的封面
(图片来源:《Science Translational Medicine》)
▌ 全球女性中最常见的癌症
乳腺癌是全球女性中最常见的癌症。据统计,在包括美国在内的一些发达国家,随着寿命的不断延长,每8名女性中,就会有1名会罹患乳腺癌。由于并非所有的乳腺癌都能在早期得到诊断,许多患者在确诊时,疾病往往已经进入了中后期,治疗效果不容乐观。在这些乳腺癌中,有一类叫做“三阴性乳腺癌”的亚型。这些乳腺癌的肿瘤表面缺乏雌激素受体(ER)、孕激素受体(PR)、以及人类表皮生长因子受体(HER2),因此常见的内分泌疗法或是抗HER2疗法对这类患者无能为力。
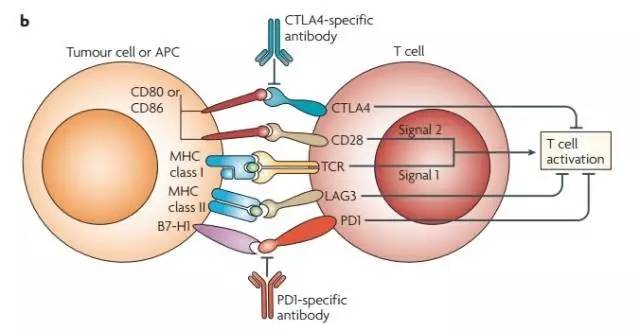
那么,肿瘤免疫疗法是否能治疗这类难治的乳腺癌呢?我们先来看看这种疗法背后的原理。目前,两类肿瘤免疫疗法药物广受关注:一类能靶向CTLA-4蛋白,一类能靶向PD-1/PD-L1通路。这两类药物也以“免疫检查点抑制剂”这一名称为人所熟知。顾名思义,“免疫检查点”是一类能对免疫系统进行自我检查,防止它过度激活的保护机制。正是由于这种保护机制的存在,人体的免疫系统才不会对自己的细胞、组织和器官进行攻击。然而,一些肿瘤细胞会利用这套机制,逃避免疫系统的监控与攻击,导致肿瘤在人体内疯狂生长。
▲多种分子会影响免疫系统对肿瘤进行攻击
(图片来源:《自然》)
可以想象,能抑制这些“免疫检查点”的药物,会擦亮免疫细胞的双眼,使它们不被肿瘤所麻痹,从而激活它们对肿瘤的杀伤能力,起到治疗癌症的效果。在肺癌、膀胱癌等癌症上,这些药物也证实了自己的潜力。至今,已有多款新药得到了美国FDA的批准上市。
但在乳腺癌的治疗上,这类突破性疗法却意外地收效甚微。为此,研究人员做出了一个假设——在其他种类的癌症中,肿瘤细胞往往会产生许多新的突变。这些突变就好像一个个“杀马特”造型,吸引了免疫细胞的注意。因此,免疫疗法在这种突变较多的癌症中,能取得不俗的战绩。然而乳腺癌则不是这样。“乳腺癌的肿瘤极少带有过量突变。”研究人员在论文中说道。这样的肿瘤细胞就好像是茫茫人海中走过的一名路人,很难引起免疫细胞的关注。
幸运的是,在三阴性乳腺癌里,研究人员发现了一个特性——这类癌症虽然不具有常见的几种治疗靶点,但却往往和BRCA突变有着关联。说起BRCA突变,关注娱乐动态的读者们想必不会陌生:这种突变会影响DNA的自我修复,导致DNA里出现错误,增加患癌的风险。好莱坞女星安吉丽娜·朱莉(Angelina Jolie)正是由于检测出自身携带的BRCA突变,才做了预防性的双乳切除术和卵巢切除术。
▲安吉丽娜·朱莉的选择一度曾引发热议
(图片来源:《自然》)
说到这里,一些读者朋友们可能发现了三阴性乳腺癌的治疗关键——乳腺癌难用免疫疗法治疗是因为肿瘤缺乏足够的新突变,但带有BRCA突变的三阴性乳腺癌,DNA发生突变的概率会上升。也许,这些新增的突变足以让免疫细胞更关注肿瘤,并让免疫疗法对乳腺癌产生效果。这也正是研究人员所设想的思路。
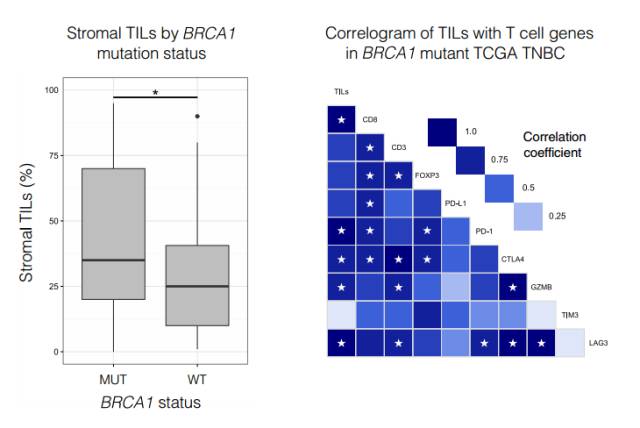
由于人们开展了大量乳腺癌的相关试验,研究人员能很快地从先前的数据中找到了支持这一思路的关键证据——在那些带有BRCA1突变的三阴性乳腺癌患者中,从肿瘤部位分离出的浸润性T细胞要显著更多,表明免疫系统对这些肿瘤的反应更为强烈。此外,这些浸润性T细胞数量的增加,也和PD-1、CTLA-4等关键基因的表达呈正相关。这些数据表明,带有BRCA1突变的三阴性乳腺癌患者,的确有潜力从肿瘤免疫疗法受益。
▲带有BRCA1突变的三阴性乳腺癌患者,肿瘤浸润T细胞数量更多(左)
浸润T细胞数量和免疫疗法有关的一些关键基因也呈正相关
(图片来源:《Science Translational Medicine》)
为了确认这个假设,研究人员在罹患三阴性乳腺癌的小鼠中同时注射了抗PD-1的抗体以及抗CTLA-4的抗体,想了解两种肿瘤免疫疗法双管齐下的疗效。然而实验结果却让他们大失所望。和对照组相比,接受肿瘤免疫疗法的小鼠生存率竟然没有显著变化!
这些结果让研究人员百思不得其解:实验失败的原因是由于肿瘤免疫疗法的剂量不够?缺少了其他关键的因素?还是因为这个假设压根就是错的?从先前的资料中,研究人员找到了一个潜在的解释——目前,乳腺癌的标准疗法包括顺铂化疗。这一分子虽然结构简单,却在多种癌症的化疗中起到了很好的效果。与此同时,学界的主流观点认为,化疗杀死的一些肿瘤细胞,会将肿瘤的抗原释放到血液内,方便免疫细胞进行识别,这反过来会增强免疫疗法的效果。或许,为了治疗这种难治的乳腺癌,单纯使用免疫疗法是不够的。
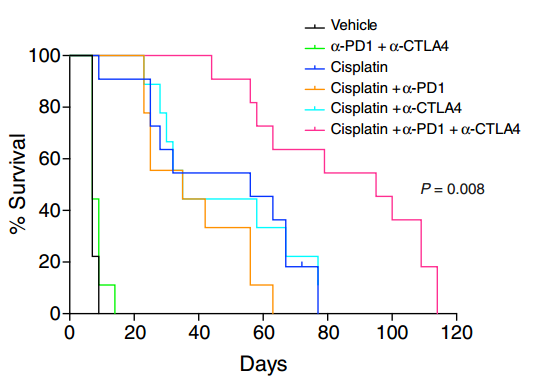
▲“三管齐下”的肿瘤免疫组合疗法(粉色)
显著延长了三阴性乳腺癌小鼠的生存期
图片来源:《Science Translational Medicine》
果不其然。在把顺铂化疗与抗PD-1的抗体、抗CTLA-4的抗体结合起来后,患有三阴性乳腺癌的小鼠的病情得到了很好的控制,效果要远胜于单独使用顺铂化疗,或是两款免疫疗法抗体药物的组合。更有趣的是,这一良好的效果需要这3种成分的共同参与。研究人员也发现,单独使用顺铂化疗+抗PD-1的抗体,或是顺铂化疗+抗CTLA-4的抗体,都无法取得很好的疗效。小鼠的生存率与顺铂化疗相差无几。
“三阴性乳腺癌与其他类型的乳腺癌相比,无法从靶向疗法中得到类似的生存率改善,”这项研究的主要负责人之一Geoffrey J. Lindeman教授说到:“我们的研究表明,通过将抗PD-1、抗CTLA-4的免疫疗法与化疗相结合,能够让与BRCA1突变有关的肿瘤停止生长,并显著延长实验室模型动物的生存期。”
▲研究人员期待他们的发现能给未来的临床试验提供一个思路
(图片来源:《Science Translational Medicine》)
研究人员们相信,这项研究说明,也许将多种肿瘤免疫疗法与化疗相结合,能够在临床试验里为患者带来更好的疗效。目前,在所能搜索到的167项与三阴性乳腺癌治疗的临床试验中,只有3项同时涉及了抗PD-1药物与抗CTLA-4药物,尚有较大的开发空间。未来,这一领域的前景值得期待。
参考资料:
[1] Combined immune checkpoint blockade as a therapeutic strategy for BRCA1-mutated breast cancer
[2] New treatment hope for women with BRCA1 breast cancers
大通福克斯美国会诊中心(CMAA)是一家专注于为中国患者提供美国高端精准医疗咨询和服务的专业机构。自成立至今,已经为许许多多的中国患者提供了这样的服务,不仅让他们体会到了高端的,专业的服务,而且接受了精准的,个体化的治疗。最重要的是,通过中心提供的服务,很多病人获得了满意的,甚至是超越他们期望的治疗效果。