▌ 导语:
日前,处于临床阶段的癌症基因疗法公司Tocagen宣布,美国FDA已授予其在研疗法Toca 511 & Toca FC突破性疗法资格认定,用于治疗复发性高级别胶质瘤(high grade glioma)。目前,Toca 511 & Toca FC已处于2/3期临床试验阶段,用于测试其对发生第一或第二次复发的胶质母细胞瘤(glioblastoma)以及正接受手术的间变性星形细胞瘤(anaplastic astrocytoma)患者的疗效。

高级别胶质瘤是最为常见和侵袭性的原发性脑癌之一,预计在2017年在全世界将有近16万新确诊患者。高级别胶质瘤的两种最常见的形式是胶质母细胞瘤和间变性星形细胞瘤。新确诊患者的标准治疗包括手术切除,然后进行放疗和化疗。然而,大多数患者即便在接受最大限度治疗后仍会复发,复发后的中位生存期通常为7至9个月。
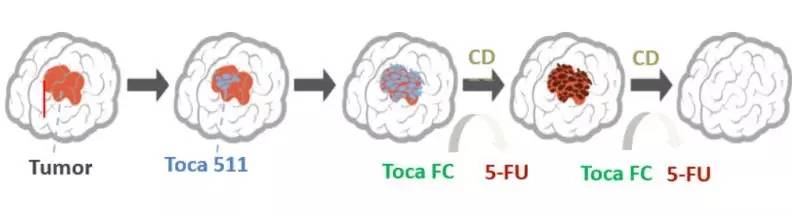
Tocagen的这一在研疗法是Toca 511(vocimagene amiretrorepvec)和Toca FC的组合。Toca 511是一种用于注射的逆转录病毒复制载体(RRV),其编码可将前药激活的胞嘧啶脱氨酶(CD),后者源自酵母,不见于人体内。在被选择性递送至癌细胞后,感染的癌细胞携带有CD基因并可产生CD酶。Toca FC则可口服,为5-氟胞嘧啶(5-FC)的缓释制剂,是抗癌药物5-氟尿嘧啶(5-FU)的无活性前药。在使用时,口服给予的Toca FC被吸收进入血液循环,并很容易穿过血脑屏障而扩散到脑部的癌细胞中。5-FC在由Toca 511感染的癌细胞内被CD酶转化为5-FU。
▲Toca 511 & Toca FC作用机理(图片来源:Tocagen官网)
以这种方式产生的5-FU具有双重作用机制:直接杀死RRV感染的癌细胞和相邻的未感染癌细胞,并且还杀死免疫抑制性细胞,例如髓源性抑制细胞(MDSC),后者是肿瘤中主要的免疫抑制因素,将其去除可促进抗肿瘤免疫应答。此外,免疫系统还会被肿瘤相关抗原和从死亡癌细胞释放的病毒蛋白进一步活化。这种方法选择性地杀死体内的癌细胞,同时保持健康的细胞不受伤害。
“FDA第一次将突破性疗法资格认定授予这种类型脑癌的疗法,突出了对这种致命疾病的新治疗选择的迫切需求,”Tocagen首席执行官Marty Duvall先生表示:“基于我们目前所看到的令人鼓舞的安全性和有效性数据,继续推动Toca 511和Toca FC的研发仍然是我们团队的首要任务。我们期待与FDA密切合作,加速该疗法的开发和审查。”
参考资料:
[1] Tocagen Receives Breakthrough Therapy Designation from U.S. Food and Drug Administration for Toca 511 & Toca FC in Recurrent High Grade Glioma
[2] Tocagen公司官网
大通福克斯美国会诊中心(CMAA)是一家专注于为中国患者提供美国高端精准医疗咨询和服务的专业机构。自成立至今,已经为许许多多的中国患者提供了这样的服务,不仅让他们体会到了高端的,专业的服务,而且接受了精准的,个体化的治疗。最重要的是,通过中心提供的服务,很多病人获得了满意的,甚至是超越他们期望的治疗效果。