据大通福克斯美国会诊中心(CMAA)了解:Seattle Genetics和安斯泰来(Astellas Pharma)今天宣布,美国FDA为抗体药物偶联物(ADC)enfortumab vedotin颁发了突破性疗法认定,用于治疗局部晚期或转移性尿路上皮癌患者。最新相关资讯信息,大通福克斯美国会诊中心(CMAA)将持续为您报道。
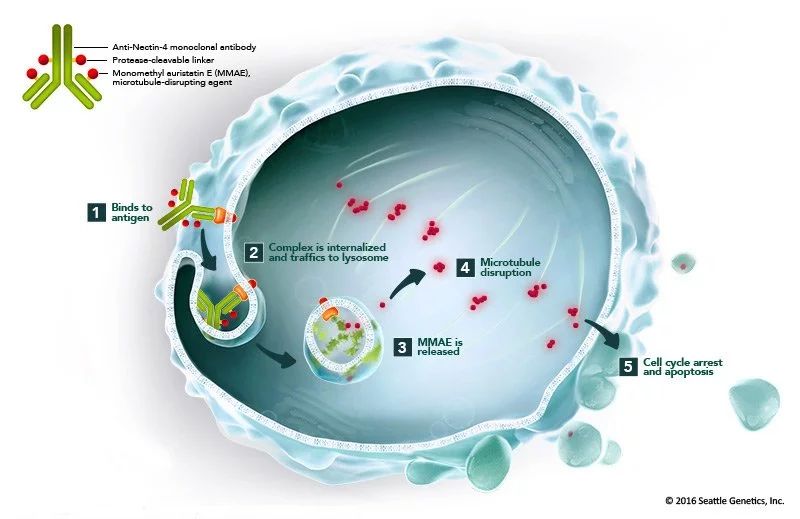
▲这款新药的潜在作用机理
尿道上皮癌最常见于膀胱(90%)。 根据美国癌症协会的统计,2017年美国约有79000人将被诊断为膀胱癌,将近17000人将死于这种疾病。确诊为转移性疾病的患者预后很差,5年生存率为5%。
Enfortumab vedotin使用Seattle Genetics的专有连接技术,将微管破坏剂MMAE和抗Nectin-4单克隆抗体连接。Enfortumab vedotin可靶向在多种实体瘤上表达的细胞粘附分子Nectin-4。
此次突破性疗法认定基于1期临床研究的中期结果,该研究将enuteumab vedotin作为接受过检查点抑制剂(CPI)治疗的转移性尿路上皮癌患者的单一疗法,主要终点是耐受性,次要终点是根据实体肿瘤疗效评价标准1.1版(RECIST v1.1),每8周一次评估抗肿瘤活性。
Enfortumab vedotin表现出良好的耐受性,在经过先前治疗,包括接受CPI失败的患者中表现出了令人鼓舞的抗肿瘤活性。所有可评估患者(n = 60)的总体缓解率(ORR)分别为40%(95%CI:27.6-53.5),接受过CPI患者的缓解率(n = 24)为46%(95%CI:25.6-67.2) ,转移至肝脏的患者为44%(95%CI:19.8-70.1)(n = 16)。在剂量≥1mg/kg时,完全缓解的患者有3例。平均治疗时间为26周(范围:5.1-64.6),中位缓解持续时间为18周(95%CI:8.4-40.1),中位无进展生存期为17周(95%CI:15.1-23.3)。
此外,Enfortumab vedotin还在一项2期关键性临床试验EV-201(NCT03219333)中,作为单独疗法,以及与CPI疗法结合的早期临床试验EV-103(NCT03288545)中进行研究。

▲Enfortumab vedotin是Seattle Genetics的领先疗法
“Enfortumab vedotin的突破性疗法认定是我们向患者带来额外治疗选择的又一进步,”安斯泰来高级副总裁,肿瘤开发全球疗法主管Steven Benner先生说:“随着enfortumab vedotin 2期试验和CPI组合疗法试验的积极开展,安斯泰来期待扩大enfeumab vedotin和其他肿瘤管道的开发,针对包括最难治疗的癌症。”
我们期待这款ADC疗法的临床试验可以顺利进行,早日为广大癌症患者带来新疗法。
参考资料:
[1] Seattle Genetics and Astellas Receive FDA Breakthrough Therapy Designation for Enfortumab Vedotin in Locally Advanced or Metastatic Urothelial Cancer
[2] FDA hands a ‘breakthrough’ designation to Seattle Genetics’ pivotal-stage cancer drug enfortumab
[3] A phase I study of enfortumab vedotin (ASG-22CE; ASG-22ME): Updated analysis of patients with metastatic urothelial cancer.
[4] 转自药明康德
大通福克斯美国会诊中心(CMAA)是一家专注于为中国患者提供美国高端精准医疗咨询和服务的专业机构。自成立至今,已经为许许多多的中国患者提供了这样的服务,不仅让他们体会到了高端的,专业的服务,而且接受了精准的,个体化的治疗。最重要的是,通过中心提供的服务,很多病人获得了满意的,甚至是超越他们期望的治疗效果。
▌ 推荐阅读
治疗更灵活!首款四周一次PD-1抑制剂获批
艾滋病组合疗法获FDA暂定批准



