▌ 导语:
神经母细胞瘤(Neuroblastoma)是一种由未成熟神经元癌变而导致的肿瘤,多发生于五岁以下儿童。肾上腺是最常见的发病地点,此外腹、胸、颈部的神经元也是潜在的病灶位点。神经母细胞瘤虽可被治愈,可一旦肿瘤发展到晚期则会带来生命危险,且即便度过了难关也可能给患儿的身体和智力发育造成终生的损害。
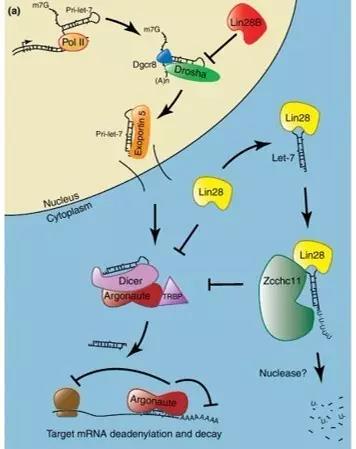
▲LIN28B对let-7的抑制作用
关于该病的病因,人们长期以来了解得并不彻底。不过,一种叫做LIN28B的蛋白被发现可引发神经母细胞瘤,通过抑制对原癌基因MYCN具有下调作用的let-7 microRNA,导致MYCN的表达量升高。let-7是一种具有抑癌作用的microRNA家族,在许多种肿瘤中缺失。它有着高度的进化保守性,其13个成员的基因分布于9个不同的染色体上。
最近,波士顿儿童医院等机构的研究者发现,let-7在神经母细胞瘤发生中可能起着比LIN28B更为中心的作用,且导致其在肿瘤中“销声匿迹”的原因不只是LIN28B蛋白。这一成果发表在最新的《Nature》期刊上,为神经母细胞瘤的治疗提供了新的参考靶点。
原来,MYCN基因在作为let-7抑制对象的同时,本身也可以反过来阻断let-7的作用。当MYCN基因出现扩增突变后,其转录出的大量mRNA足以冲淡let-7的“存在感”,使其在肿瘤细胞中的活动受到极大地限制。这一过程是完全独立于LIN28B蛋白的。
“25%的神经母细胞瘤患儿携带MYCN基因扩增突变,这些患儿的预后往往是最差的,”文章的第一作者、波士顿儿童医院的John T. Powers博士说道:“长久以来,神经母细胞瘤研究领域的一个大问题便是‘为什么会有这么多的MYCN mRNA’。现在我们知道,如此巨量mRNA足以冲淡let-7的影响。”
此外,研究者还发现,let-7基因的缺失突变可以引发神经母细胞瘤。不仅如此,在参与该研究的202名神经母细胞瘤患者中,凡是带有let-7缺失突变的患者几乎都不会出现MYCN基因的异常扩增。这说明,二者是完全相互独立,甚至带有一型互斥性的致癌机理。
研究者认为,人为上调let-7水平可作为一种低副作用的神经母细胞瘤新型治疗思路,并可能同样适用于出现let-7缺失的其他肿瘤类型。let-7 microRNA本身甚至就可以作为抗肿瘤药物,只要人们能找到有效的递送方法。另一方面,LIN28B、MYCN、let-7三者也有望用于神经母细胞瘤的诊断,并为该病的个体化治疗提供基础。此外,这一结果还表明,目前的神经母细胞瘤小鼠模型仍有待改进,因为没有反映let-7 microRNA在该肿瘤中的情形。
“我们发现,let-7的抑制在神经母细胞瘤的发生中发挥了关键角色,” John T. Powers博士说道:“这是如此的关键,以至于该肿瘤需要演化出至少三种手段以实现它。”
参考资料:
[1] Loss of a microRNA family, let-7, found key in neuroblastoma
[2] Multiple mechanisms disrupt the let-7 microRNA family in neuroblastoma
[3] The role of let-7 in cell differentiation and cancer
[4] LIN28B induces neuroblastoma and enhances MYCN levels via let-7 suppression
[5] Wikipedia: Neuroblastoma
大通福克斯美国会诊中心(CMAA)是一家专注于为中国患者提供美国高端精准医疗咨询和服务的专业机构。自成立至今,已经为许许多多的中国患者提供了这样的服务,不仅让他们体会到了高端的,专业的服务,而且接受了精准的,个体化的治疗。最重要的是,通过中心提供的服务,很多病人获得了满意的,甚至是超越他们期望的治疗效果。



